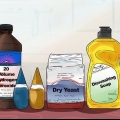
Le chlorure de sodium (ou sel de table) est un électrolyte qui contribue à améliorer la conductivité de l`eau. L`eau en elle-même n`est pas un très bon conducteur. En améliorant la conductivité de l`eau, l`électricité de la batterie la traverse plus facilement, de sorte que l`eau est mieux divisée en hydrogène et oxygène. 
Les mines de graphite dans les crayons agissent comme des électrodes et conduiront l`électricité provenant de la batterie. Le graphite est très approprié car il ne se dissoudra pas ou ne sera pas endommagé par l`eau pendant l`expérience. 
Le morceau de carton permet de laisser pendre les mines de graphite des crayons dans l`eau sans toucher le côté du verre. Le carton n`a aucune des propriétés du métal, il peut donc reposer sur le verre sans affecter le résultat de l`expérience. 


En faisant cela, la connexion à la batterie est complète et le courant électrique de la batterie peut être libéré dans l`eau. 
Pour que cette expérience fonctionne, le graphite des crayons ne doit pas toucher le côté du verre. Vérifiez donc à nouveau et déplacez les crayons si nécessaire. 
Lorsque vous connectez les pinces crocodile à la batterie et au graphite, l`électricité commence à se déplacer immédiatement. Plus de bulles proviennent de l`hydrogène gazeux car chaque molécule d`eau contient deux fois plus d`hydrogène que d`oxygène.
Faire de l'hydrogène et de l'oxygène par électrolyse
Teneur
Le processus par lequel l`eau (H2O) est décomposé en différents types d`atomes ou d`éléments (hydrogène et oxygène) à l`aide d`électricité est appelé électrolyse. Cette expérience a des implications importantes pour les applications de ces deux gaz, l`hydrogène étant l`une des sources d`énergie les plus propres auxquelles nous ayons accès. Cela peut sembler compliqué, mais c`est plus facile que vous ne le pensez si vous avez les bonnes ressources, connaissances et compétences.
Pas
Partie 1 sur 2 : Mise en place de l`expérience

1. Remplir un verre de 350 ml d`eau tiède. Vous n`êtes pas obligé de remplir le verre à ras bord, alors laissez de l`espace. Lorsque l`eau est chaude, elle conduira mieux l`électricité. Cependant, cette expérience fonctionne également bien avec de l`eau froide.
- Vous pouvez utiliser de l`eau du robinet ou de l`eau en bouteille. Peu importe ce que vous choisissez.
- L`eau plus chaude a un viscosité et permet aux ions conducteurs d`électricité de se déplacer plus librement.

2. Dissoudre 1 cuillère à soupe (20 grammes) de sel de table dans l`eau. Il vous suffit de verser le sel dans l`eau et de remuer un peu l`eau pour vous assurer que le sel se dissout. Vous avez maintenant une solution saline.

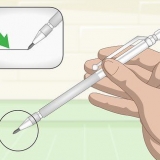
3. Aiguisez 2 crayons HB aux deux extrémités pour que vous puissiez voir le graphite. Assurez-vous de retirer la gomme au bout du crayon. Vous devrez affûter les crayons suffisamment pour que le graphite soit entièrement exposé aux deux extrémités.

4. Découpez un morceau de carton carré assez grand pour couvrir le verre. Utilisez du carton suffisamment épais et qui restera ferme lorsque vous y ferez des trous. Par exemple, découpez un carré dans une boîte à chaussures ou une autre boîte de carton épais.

5. Percez 2 trous dans le carton avec les 2 crayons. Utilisez les crayons eux-mêmes pour cela, car ils doivent rester fermement dans les trous afin qu`ils ne bougent pas ou ne coulent pas. Si le graphite heurte le côté ou le fond du verre, l`expérience sera interrompue.
Partie 2 sur 2: Exécution de l`expérience

1. Connectez les extrémités des pinces crocodiles aux bornes de la batterie. La batterie est l`endroit d`où vient l`énergie électrique et les pinces crocodiles garantissent que cette énergie est transportée jusqu`à l`eau. Attachez une pince crocodile à la borne positive et une pince crocodile à la borne négative.
- Utilisez une batterie de 6 volts pour cela. Si vous ne le trouvez pas, utilisez une pile 9 volts.
- Vous pouvez acheter ce type de batterie dans presque tous les supermarchés et grands magasins.

2. Attachez les autres extrémités des pinces crocodiles aux crayons. Assurez-vous que la partie métallique de la pince crocodile touche le graphite du crayon. Vous devrez peut-être couper un peu de bois dans les crayons pour vous assurer que les pinces crocodiles entrent pleinement en contact avec le graphite.

3. Placez le morceau de carton sur le verre pour que les crayons soient immergés sous l`eau. En raison de la façon dont vous venez de couper le carton, il devrait maintenant rester bien au-dessus du verre. Essayez de le faire avec précaution afin que les crayons qui traversent le carton ne bougent pas ou ne glissent pas.

4. Regardez comment l`eau se décompose en hydrogène et oxygène. Des bulles devraient maintenant s`élever des points submergés de graphite. Cela signifie que l`hydrogène gazeux et l`oxygène gazeux sont séparés. De l`hydrogène gazeux monte du crayon connecté à la borne négative et de l`oxygène gazeux monte du crayon connecté à la borne positive.
Des astuces
- Si vous ne trouvez pas de crayons avec une mine de graphite, vous pouvez également utiliser de courtes longueurs de fil. Enroulez une extrémité autour de la batterie et mettez l`autre extrémité dans l`eau. Cela a le même effet que d`utiliser des crayons.
- Utiliser une batterie avec une tension différente. Cela affecte la quantité de courant électrique qui traverse l`eau, qui à son tour affecte la vitesse à laquelle les molécules d`eau sont divisées.
Mises en garde
- Si vous utilisez un électrolyte comme sel pour améliorer la conductivité, sachez qu`une petite quantité de chlore est produite comme sous-produit. Ce n`est pas suffisant pour être dangereux, mais vous pouvez sentir une légère odeur de chlore.
- Effectuez cette expérience sous la surveillance d`un adulte car vous travaillerez avec de l`électricité et des gaz qui, aussi improbables soient-ils, pourraient vous être nocifs.
Nécessités
- 2 crayons HB
- 1 pile 6 ou 9 volts
- Verre d`une contenance de 350 ml
- 2 pinces crocodiles
- Taille-crayon
- sel de table
Articles sur le sujet "Faire de l'hydrogène et de l'oxygène par électrolyse"
Оцените, пожалуйста статью
Populaire